|
|
撰文︱王思珍
责编︱王思珍
亲爱的读者朋友们,近期,我们将精选一些Nature、Cell、及Science的神经科学领域的最新优秀综述文章,供大家及时学习。
本期,我们特别推荐Nature子刊Nature Reviews Neurology的相关综述文章,共7篇(2020年7-8月份)【即Nature神经科学领域7-8月份最新综述精选 (一)】,以小概要的形式分享给大家,详细内容可自行下载原文后阅读。
主要内容包括:CRISPR筛选技术揭示神经系统疾病的发病机制和治疗靶点;郎飞氏结在中枢神经系统中的发育和修复机制;COVID-19流行期间的神经免疫疗法共识;机器学习在神经退行性疾病诊断和治疗中的应用;亨廷顿病的分子发病机制和治疗机会的新见解;人工智能在急性中风中的决策支持(包括目前的作用和潜力);COVID-19、炎症和衰老的背景下的神经免疫单元概念、以及疾病治疗策略。

神经退行性疾病、神经发育疾病和神经精神疾病是公共卫生面临的最大挑战,这是因为目前这些疾依旧缺乏有效治疗。其中的一个主要原因是我们对病因分子和细胞机制的认识很十分有限。全基因组关联研究揭示出很多疾病相关的遗传变异,下一个挑战则是阐明这些变异如何导致疾病,并将这些结果转化为治疗。在于2020年7月8日以CRISPR-based functional genomics for neurological disease为题代表在Nature Reviews Neurology上的综述文章中,美国加州大学旧金山分校神经退行性疾病研究所的Martin Kampmann教授综述了最新基于CRISPR技术的功能基因组学方法帮助如何揭示神经系统疾病的发病机制和治疗靶点。细菌CRISPR系统可用于实验疾病模型中,并通过CRISPR干扰(CRISPRi)和CRISPR激活(CRISPRa)来编辑基因组、以及控制基因的表达水平。这些遗传干扰可以在大量的平行遗传筛选中进行操作,评估人类细胞的功能结果。一些证据表明,CRISPR筛查与诱导多能干细胞技术的相结合后的效果更为强大;通过诱导多能干细胞技术,我们可以能够从患者的细胞中提取出分化的特定细胞类型,如神经元、神经胶质和脑器官。而通过CRISPRi和CRISPRa则可以建立疾病相关基因表达变化模型,揭示原因变化。此外,遗传修饰因子筛选可用于阐明疾病机制和细胞类型选择脆弱性的因果决定因素,并确定治疗靶点。
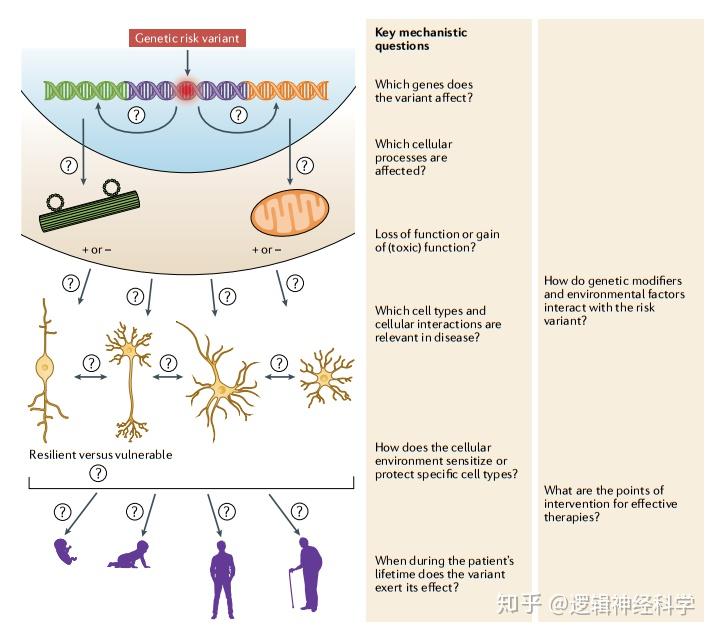
神经系统疾病的关键机制问题(图片引自:Kampmann, M. Nat Rev Neurol 2020. 16:465–480)
原文链接:
https://www.nature.com/articles/s41582-020-0373-z

动作电位(action potentials)沿着髓轴突的跳跃性传导依赖于郎飞氏结(nodes of Ranvier),郎飞氏结是一段小的未被髓鞘化的轴突区域,电压门控钠通道集中于此。我们对这些轴突结构域复杂的分子组成的认识在不断积累,在周围神经系统中已经阐明了结节的组装机制,然而在中枢神经系统中的结节组装机制,我们知之甚少。研究表明,除了结节在加速传导中起关键作用之外,结节的变化能够允许对轴突传导速度进行微调,以满足信息加工的需要。此外,研究发现,通过结节与神经胶质细胞的多种接触,结节似乎对神经元-神经胶质细胞的相互作用很重要。轴突结构域的紊乱在各种神经系统疾病的病理生理学中都有涉及。例如,在多发性硬化症中,脱髓鞘后,结节和周围结节的破坏会导致轴突传导和轴突完整性的改变,而且这种破坏伴随着离子通道分布的改变。郎飞氏结群再生的同时,髓鞘也在再生,但是结节群再生会早于髓鞘再生,这种过程中,神经轴突传导得以恢复。2020年7月10日,法国巴黎索邦大学Catherine Lubetzki教授及其同事在Nature Reviews Neurology上撰写了题目为Nodes of Ranvier during development and repair in the CNS的综述文章。作者回顾了目前关于郎飞氏结在中枢神经系统中的组织和功能方面的最新知识。紧接着,作者讨论了脱髓鞘和再髓鞘过程中结节的动态变化,并强调了这些变化对健康和疾病中的神经生理的影响,以及相关的治疗意义。
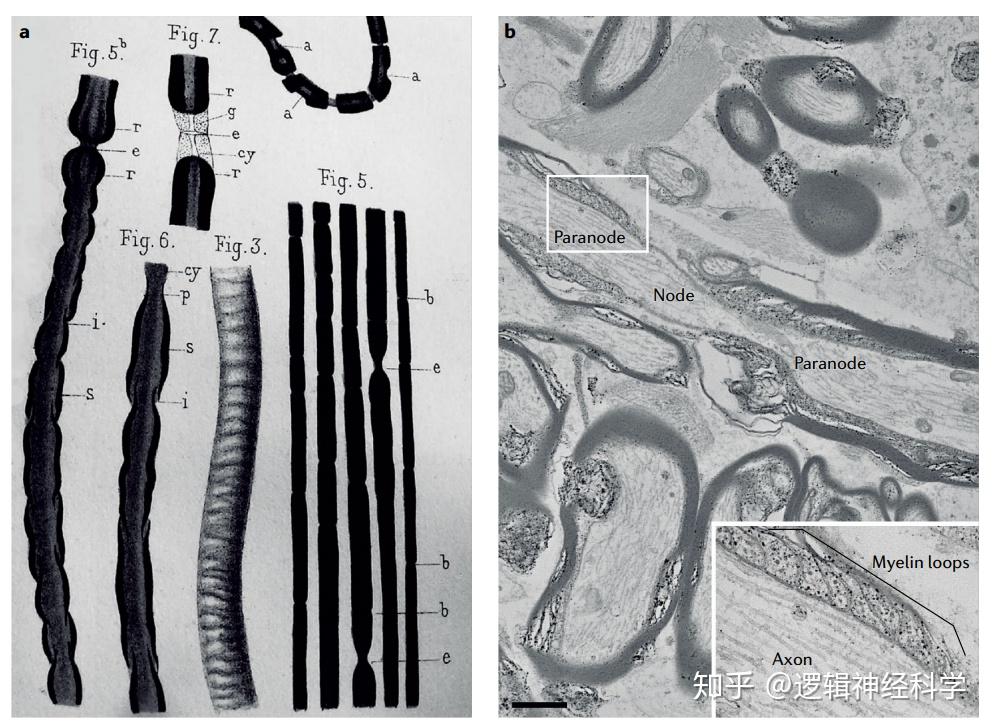
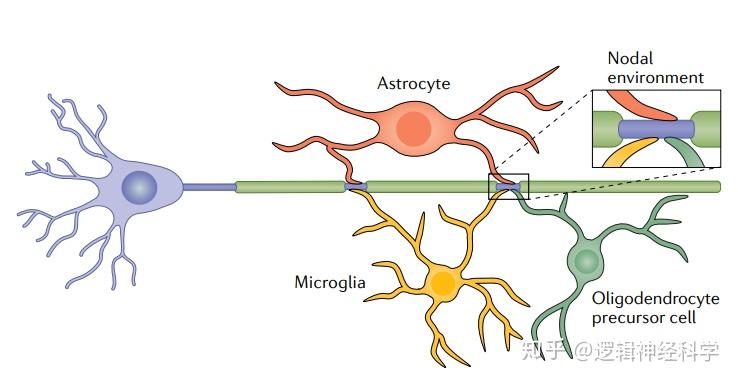
郎飞氏结(上图)郎飞氏结的神经胶质相互作用(下图)(图片引用:Lubetzki, C., et al., Nat Rev Neurol, 2020, 16: 426–439)
原文链接:
https://www.nature.com/articles/s41582-020-0375-x

新型冠状病毒肺炎(the coronavirus disease 2019,简称COVID-19)的大流行逐渐引起神经免疫性疾病(比如多发性硬化)患者的关注与担心,这些患者正在接受免疫治疗。免疫疗法能够影响感染的风险,有些疗法与来自特定类型病原体的风险增加有关。免疫疗法是否增加感染SARS-CoV-2(即严重急性呼吸系统综合征2型冠状病毒)的风险,亦或者是增加感染后所出现的严重疾病和疾病死亡的风险,目前仍不确定。许多国家、及国际社会已经制定了准则和声明,但是在若干领域还尚未达成共识。在这篇综述中,德国明斯特大学转化神经学研究所的Heinz Wiendl博士和其同事尝试阐明在哪些方面存在共识,哪些方面仍然存在不确定性,进而完善以神经免疫学核心原则为基础的科学管理办法。作者总结了文献中已解决了的关键问题,并整理出了相关建议,从而以一种类似于德尔菲法的策略来生成共识计算、总结信息【注:德尔菲法(Delphi Method)本质上是一种反馈匿名函询法,其大致流程是在对所要预测的问题征得专家的意见之后,进行整理、归纳、统计,再匿名反馈给各专家,再次征求意见,再集中,再反馈,直至得到一致的意见】。此外,作者总结了国际上的建议,并根据接受免疫治疗的COVID-19患者的首批数据进行了讨论,也对COVID-19时代的管理方法进行了概述。Heinz Wiendl等人强调了一般医学的原则,特别是神经免疫学的原则,因为尽管病毒感染的风险已经变得更加相关,但是大多数考虑适用于神经免疫治疗的一般管理。最后,作者还特别探讨了免疫抑制治疗和细胞消耗治疗,这类治疗策略可以会增加SARS-CoV-2感染的敏感性,但却可以降低感染严重COVID-19的风险。该篇综述已于2020年7月8日以Neurological immunotherapy in the era of COVID-19 — looking for consensus in the literature为题发表于Nature Reviews Neurology。
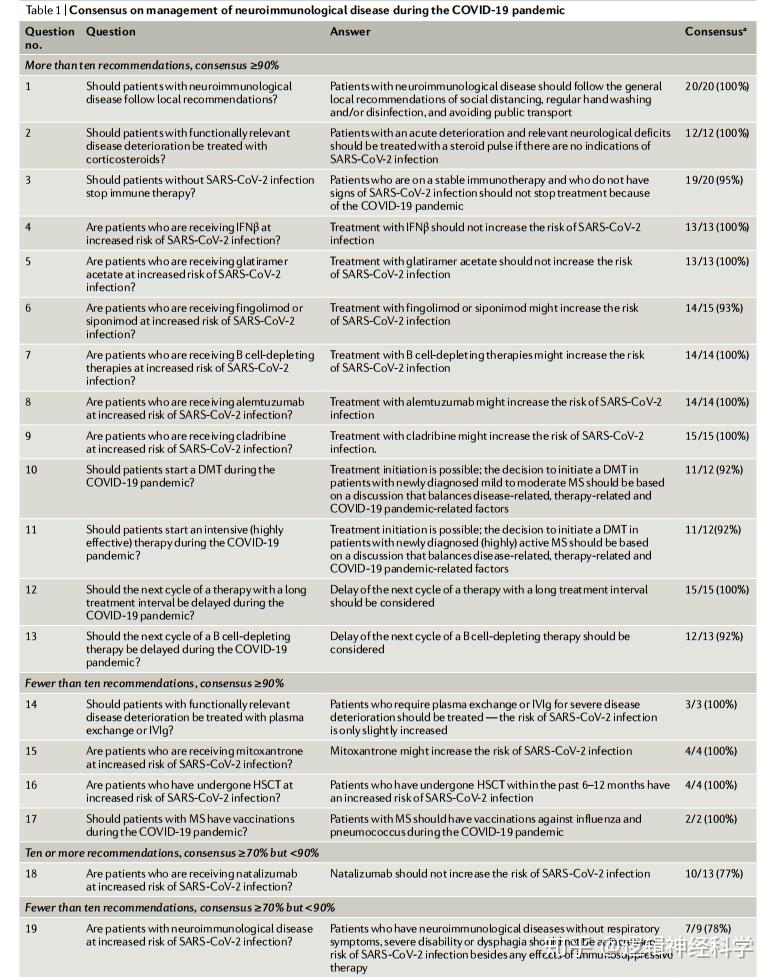
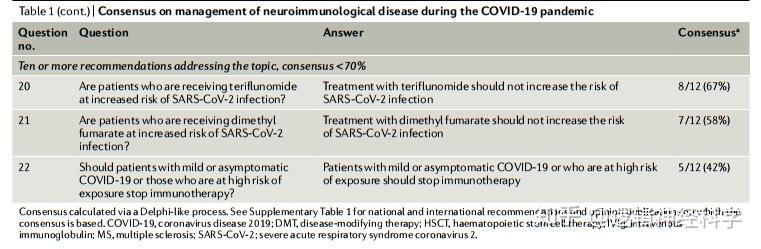
关于COVID-19大流行期间的神经免疫疾病管理的共识(图片引自:Korsukewitz, C., et al. Nat Rev Neurol , 2020, 16: 493–505)
原文链接:
https://www.nature.com/articles/s41582-020-0385-8

在全球范围内,神经退行性疾病的有效治疗仍然未被满足,且存在着巨大的治疗需求。神经变性的复杂分子机制和患者群体的异质性给这些疾病的早期诊断工具、及有效治疗的开发带来了巨大的挑战。机器学习(machine learning)作为人工智能的一个分支领域,可以帮助科学家、临床医生以及患者应对其中一些挑战,包括发病机制、疾病诊断与治疗等。在这篇综述中,英国谢菲尔德大学谢菲尔德转化神经科学研究所Laura Ferraiuolo教授及其同事讨论了机器学习如何帮助对医学影像的早期诊断和解释,以及新疗法的发现与发展。虽然机器学习有着不同应用,但是一个统一的主题是对多个高维度数据源进行有效整合,继而提供了对疾病的不同看法,以及可操作的见解或观点的出现。该篇综述已于2020年7月15日发表于Nature Reviews Neurology,题目为Applications of machine learning to diagnosis and treatment of neurodegenerative diseases。
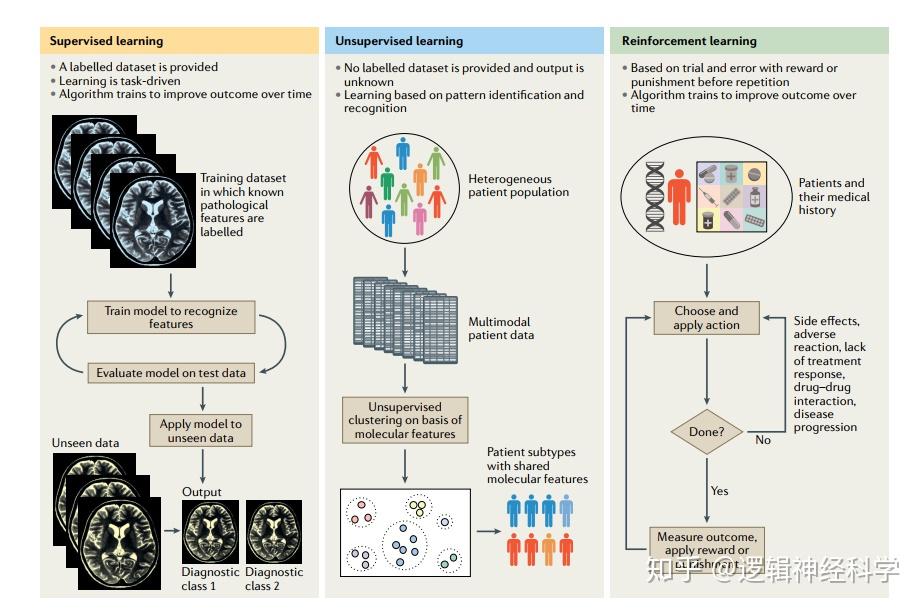
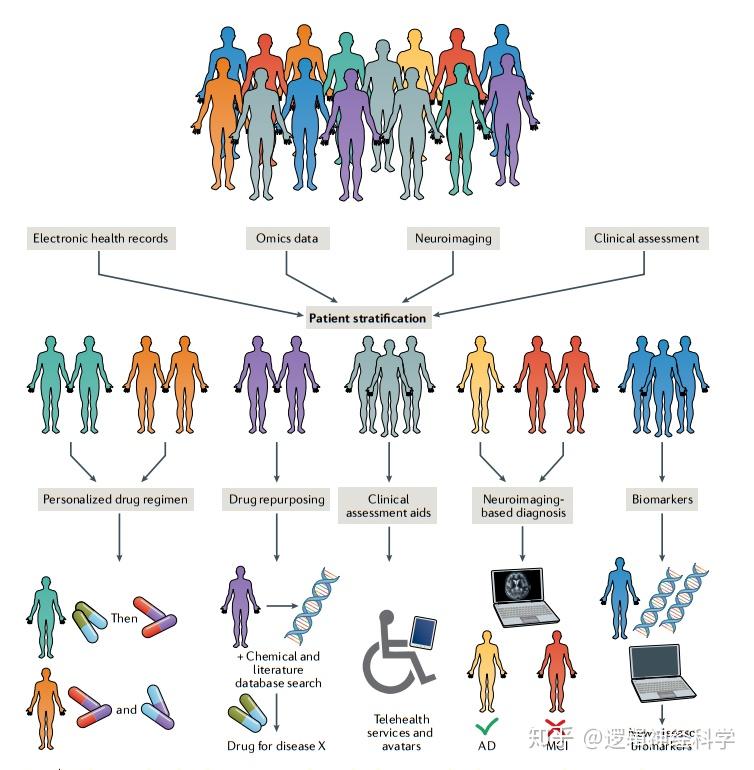
机器学习的类别(上图),机器学习方法在神经退行性变治疗的发展和实施中的应用(下图)(图片引用:Myszczynska, M.A.,et al., Nat Rev Neurol, 2020, 16: 440–456)
机器学习的类别(上图),机器学习方法在神经退行性变治疗的发展和实施中的应用(下图) (图片引用:Myszczynska, M.A.,et al., Nat Rev Neurol, 2020, 16: 440–456)
原文链接:
https://www.nature.com/articles/s41582-020-0377-8

亨廷顿病(HD)是一种由亨廷顿基因(HTT)中CAG重复扩增而引起的神经退行性疾病,且发病机制复杂。HTT蛋白突变体(mHTT)会扰乱转录,干扰免疫和线粒体的相关功能,并在翻译后发生异常修饰。有证据表明,mHTT的RNA是有毒的,从DNA水平上来看,体细胞CAG重复扩张会影响疾病过程。全基因组关联研究已确定,在HD和其他重复扩增疾病中,DNA修复通路能够作为体细胞不稳定和病程的调节剂。在HD动物模型中,核质运输被破坏,而其功能恢复则具有神经保护。在前期HD个体中,新型脑脊液和血浆生物标志物是最早检测到的变化,并具有一定敏感性,这提示了治疗效益。而在治疗方面,首个降低反义寡核苷酸的人体试验已取得成功,并且能够安全地降低了HD患者脑脊液中mHTT的浓度。此外,一项更大规模的试验正在进行,旨在进一步检测临床疗效;此外,其他降低HTT的一些方法也在进行中。在这篇综述中,英国伦敦大学学院亨廷顿病中心的Sarah J. Tabrizi教授和Michael D. Flower博士等人综述了HD分子发病机制的新见解和未来的治疗策略,作者特别强调了DNA修复调控和DNA突变本身的靶向。此文章已于2020年8月14日以Huntington disease: new insights into molecular pathogenesis and therapeutic opportunities为题在线发表于Nature Reviews Neurology。
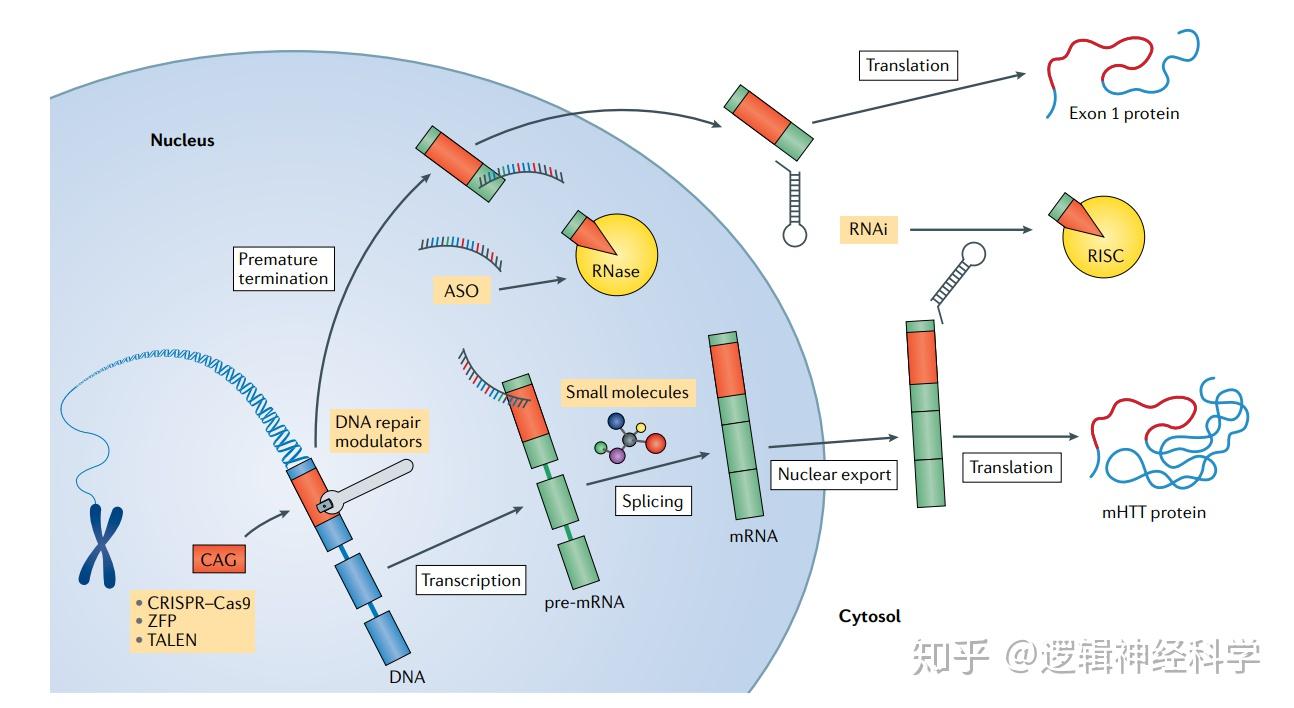
降低HTT蛋白表达的治疗方法(图片引自:Tabrizi, S.J., et al. Nat Rev Neurol, 2020)
原文链接:
https://www.nature.com/articles/s41582-020-0389-4

随着越来越多的治疗选择的出现,以及疾病特征和治疗反应之间的新关系不断被发现,对中风患者的鉴别和治疗正变得越来越复杂。因此,临床医生必须不断学习新技能(如临床评估或图像判读),及时阅读最新文献,并将新知识和技能融入日常实践。人工智能(AI)可以支持临床决策,减少常规临床实践中评分者之间的差异,并有助于提取重要信息,从而提高对中风患者的鉴别,预测治疗反应和患者结局。这种AI支持系统,对于处理局部区域的极少数中风病人来说是理想的,并且可以帮助与病人及其家属进行病情讨论。此外,利用人工智能进行脑卒中图像处理和判读,可以为临床医生提供与专家相当的影像学评估。然而,任何基于AI决策支持系统都应该允许临床医生之间的交流,鉴别错误(例如,在自动图像处理中一些错误)。在这篇综述中,澳大利亚墨尔本大学医学和公共卫生学系的Mark Parsons教授等人讨论了影像学在脑卒中治疗中的日益重要性,以及AI决策支持的潜力和缺陷;同时,作者也认为,任何决策辅助工具都必须要经过实际检验和适当地应用,并且需要明确的指导方针来定义系统在临床实践中的作用。该篇综述已于2020年8月24日发表于Nature Reviews Neurology,题目为Artificial intelligence for decision support in acute stroke — current roles and potential。
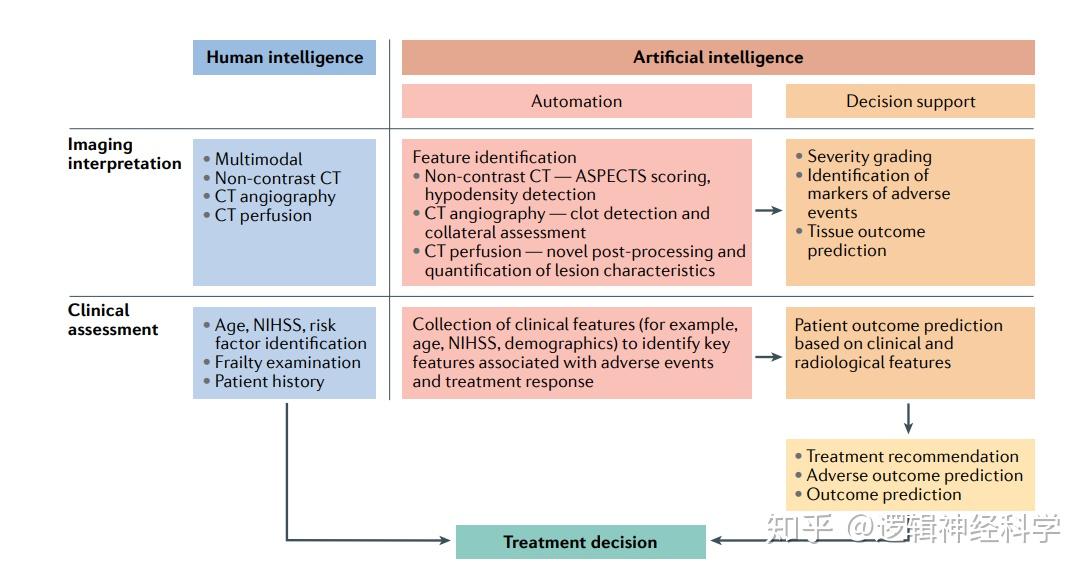
人类单独、及人类结合AI做出的治疗决策(图片引自:Bivard, A., Churilov, L. & Parsons, M. Nat Rev Neurol, 2020)
原文链接:
https://www.nature.com/articles/s41582-020-0390-y

COVID-19是由冠状病毒SARS-CoV-2引起的传染病,于2019年12月在中国武汉首次被报道以来,已引发全球大流行。急性呼吸窘迫综合症(ARDS)是COVID-19严重形式的常见特征,可导致呼吸衰竭,特别是老年人。越来越多的人认识到SARS-CoV-2的嗜神经性潜能,这引发了人们对神经系统在COVID-19患者呼吸衰竭中的作用的兴趣。然而,在ARDS背景下肺内的神经免疫相互作用尚不清楚。在于2020年8月25日以Lung innervation in the eye of a cytokine storm: neuroimmune interactions and COVID-19为题发表在Nature Reviews Neurology上的观点文章(Perspective)中,英国伦敦帝国理工学院神经科学部Francesco De Virgiliis博士和Simone Di Giovanni博士共同提出了神经免疫单元的概念,即在COVID-19、炎症和衰老的背景下,神经免疫单元是肺功能的关键决定因素,作者还特别关注了迷走神经的参与。此外,作者讨论了一些减少组织炎症、防止呼吸衰竭的方法,如神经刺激和药物神经调节。
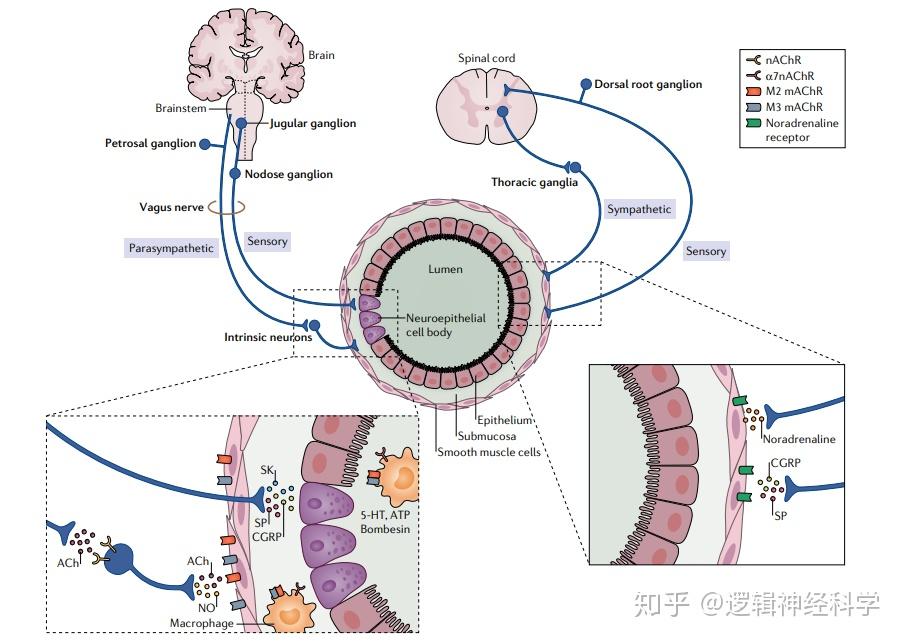
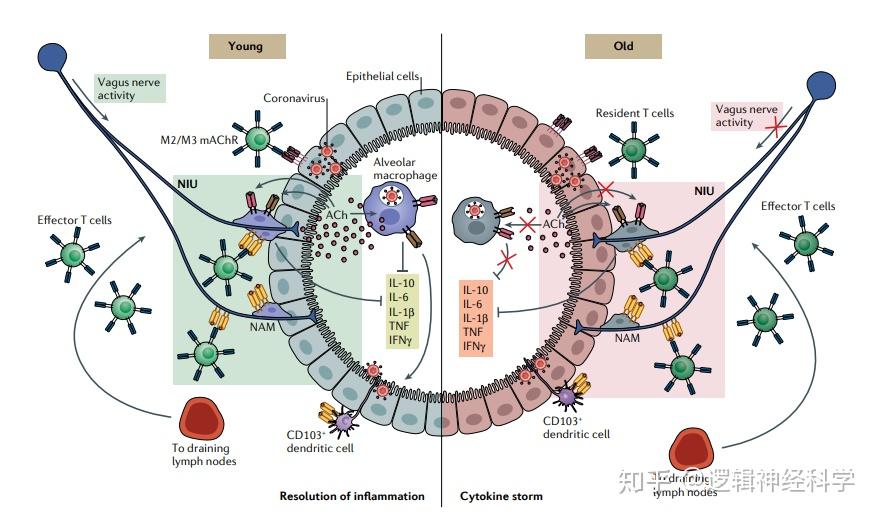
呼吸道的神经支配(上图)和神经免疫单元(下图)(图片引自:De Virgiliis, F., Di Giovanni, S. Nat Rev Neurol, 2020)
原文链接:
https://www.nature.com/articles/s41582-020-0402-y
欢迎加入逻辑神经科学: 学术群
我们不定期推荐/分享神经科学领域的优质最新讲座/会议
(添加主编微信(ID: LT-Neuroscience1)申请进群)
(备注格式:姓名-单位-研究领域-学位/职称/称号/职位)
制版︱王思珍
本文完
我们还组建了多个社群,包括学术群、出国留学群、人才招聘群、科研培训群、商业合作群、以及相关领域的其他微信群等。欢迎大家实名制添加管理员微信(ID: LT-Neuroscience1)申请进群。
我们也真诚寻求长期合作者(写作、运营;投稿及商务合作等),期待加入我们团队。
扫码关注神经学术(NeuoResearch)
掌握最新神经科学领域动态
公众号ID:NeuoResearch
关注逻辑神经科学
以严谨的学术逻辑思维,探索神经科学之奥秘
公众号ID:LT-Neuroscience |
|